1.
Latar Belakang
Polisakarida memiliki banyak manfaat salah satunya
sebagai antitumor, antioksidan, dan antiinflamasi (Huang et al., 2015; Mao et al.,
2015; Yang and Zhang, 2009). Karena itu perlu dilakukan analisa komposisi
monosakarida untuk mengetahui struktur polisakarida yang kompleks. Tantangan
menganalisa monosakarida diantaranya yaitu kesulitan dalam memisahkan,
mendeteksi, melakukan derivatisasi asam uronat, dan mendapatkan monosakarida
netral serta asam uronat (Zhang et al.,
2012). Dibandingkan dengan metode analisa lain, analisa menggunakan GC paling
banyak dipilih karena lebih akurat, presisi, sensitif dan efisien (Wang et al., 2017).
2. Metode
2.1 Standard
dan Reagen
Standard yang digunakan untuk
monosakarida netral yaitu L-ramnosa, D-arabinosa, L-fukosa, D-xylosa, D-manosa,
D-glukosa, D-galaktosa (1,5 mg/mL). Standard yang digunakan untuk asam uronat
yaitu L-asam glukuronat dan L-asam galakturonat (2 mg/mL). Reagen yang
digunakan yaitu natrium borohidrat (NaBH4), cation-exchange resin
(Amberlite 732) dan trifluoroacetic acid (TFA) sebagai pelarut. Pada penelitian
ini digunakan apple pomace pectic polysaccharide
(APP-P), Grassleaf Sweelflag Rhizone
polysaccharide (GSR-P), Agrimonia
Pilosa Ledeb polysaccharide (APL-P), lactic
acid bacteria exopolysaccharides (EPS), dan pretreatment effluent of biomass (PEB-P) untuk memverifikasi
aplikasi metode pada penelitian ini (Wang et
al., 2017).
2.2 Derivatisasi
Monosakarida dan Asam Uronat
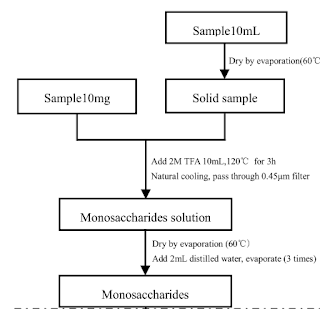
Derivatisasi dilakukan tiga tahap proses
dengan rincian pada Tabel 1 berikut:
Tabel 1. Tahap-tahap pretreatment derivatisasi
Monosakarida dan Asam Uronat
Tahap
|
Diagram Alir Proses
|
Keterangan
|
Hidrolisis
polisakarida
|
Pada
tahap ini sampel padat polisakarida dihidrolisa menjadi monosakarida dengan
cara direndam dalam 10mL larutan trifluoroacetic acid (TFA) 2M.
|
|
Reduksi gugus aldehid
|
Pada
tahap ini terjadi hidrolisis lakton yang merupakan tahap penting sebelum
reduksi. Asam aldonat dikonversi menjadi aldonolakton agar dapat bereaksi
dengan n-propylamine dan asetat anhidrida
|
|
Amidasi
dan asetilasi
|
Asam
uronat akan dikonversi menjadi n-propylamine dan monosakarida akan dikonversi
menjadi alditol asetat, sehingga dapat dianalisa menggunakan GC-FID
|
2.3 Kromatografi
Gas yang Digunakan
Kolom yang digunakan yaitu kolom
kapiler jenis high performance capillary column, DB-17 (panjang 30 m, diameter
internal 0,25 mm, ketebalan fase diam 0,25 mm, Agilent). Suhu injektor 250oC
dan suhu detektor 280oC. Jumlah sampel yang diinjeksi 1 վL
tanpa splitting. Gas pembawa yang digunakan yaitu N2 dengan
kecepatan alir 1,5 mL/menit. Hidrogen sebagai gas pendorong dengan kecepatan
alir 60 mL/menit. Udara sebagai gas pembakar untuk detektor Flame Ionization
Detector (FID) dengan kecepatan alir 450 mL/menit. Terdapat dua suhu yang
diatur untuk memisahkan derivat monosakarida yaitu:
a.
TP-A (Temperature Program-A): suhu
awal 180oC dipertahankan
selama 2 min,
kemudian dinaikan hingga 210oC dengan gradien linear setiap
5 menit dan dipertahankan selama 2 menit. Suhu kemudian dinaikkan kembali
sebesar 0,3oC/ menit
hingga mencapai suhu 215oC dan dipertahankan selama 20 menit.
Setelah itu suhu dinaikan kembali sebesar 6oC/
menit
ke suhu akhir 240oC dan dipertahankan sealama 10
menit, sehingga total waktu proses yaitu 60 menit.
b.
TP-B (Temperature Program-B): pengaturan suhu
pada TP-B sama dengan TP-A hingga suhu 215oC. Setelah
itu suhu dinaikan sebesar 8oC/menit hingga 240oC dan
dipertahankan selama 17 menit, sehingga total waktu proses yaitu 45 menit.
3. Hasil
dan Pembahasan
Hasil pengujian menggunakan GC-FID
pada kromatogram di Gambar 1 menunjukkan
bahwa sembilan derivat monosakarida dapat terpisah dengan baik. Pada suhu 215oC
dan waktu proses 45 menit, tujuh monosakarida netral dan dua asam uronat sudah
dapat terpisah dan tidak ada perbedaan signifikan antara TP-A dan TP-B. Namun
TP-B dipilih untuk analisa GC karena waktu proses yang lebih pendek daripada
TP-A.
Gambar 1. Kromatogram GC-FID campuran standard (A), APP-P (B), GSR-P (C), APL-P (D), ESP (E) and PEB-P (F). Peak pada kromatogram: (1) Ramnosa; (2) Fukosa; (3) Arabinosa; (4) Xylosa; (5) Manosa; (6) Glukosa; (7) Galaktosa; (8) Asam Glukoronat; (9) Asam Galakturonat
Berdasarkan gambar 1. ditunjukkan bahwa sampel APP-P tidak terdapat asam
glukoronat. Pada sampel GSR-P hanya terdapat monosakarida jenis arabinosa,
glukosa, galaktosa. Pada sampel APL-P hanya terdapat monosakarida jenis ramnosa,
arabinosa, glukosa, galaktosa. Pada sampel ESP terdapat monosakarida jenis arabinosa,
manosa, glukosa, galaktosa. Sedangkan sampel PEB-P mengandung monosakarida
jenis ramnosa, arabinosa, xylosa, manosa, glukosa, dan galaktosa.
Tabel 2. Retention Monosakarida dan Asam Uronat
Urutan
Peak
|
Jenis
Monosakarida
|
Retention
Time (menit)
|
Kandungan/mg
|
1
|
Ramnosa
|
11,839
|
0,2364
|
2
|
Fukosa
|
12,349
|
0,0006
|
3
|
Arabinosa
|
12,559
|
0,1820
|
4
|
Xylosa
|
13,240
|
0,1205
|
5
|
Manosa
|
23,392
|
0,0020
|
6
|
Glukosa
|
24,095
|
0,1528
|
7
|
Galaktosa
|
24,705
|
0,1419
|
8
|
Asam
Glukoronat
|
36,605
|
Tidak terdeteksi
|
9
|
Asam
Galakturonat
|
38,532
|
4,1235
|
Tabel
2. menunjukkan bahwa monosakarida jenis ramnosa memiliki Retention Time
(RT) terpendek (11,839 menit) sedangkan asam galakturonat memiliki RT
terpanjang yaitu (38,532 menit). Asam galakturonat merupakan komponen dengan
kandungan tertinggi di dalam sampel yaitu 4,1235. Sedangkan asam glukuronat
merupakan komponen dengan kandungan terendah karena itu tidak terdeteksi. Hal
ini dipengaruhi beberapa hal diantaranya:
a. Derivatisasi: Derivatisasi bertujuan
agar sampel bersifat volatil sehingga dapat dideteksi dan dipisahkan oleh GC.
Pada penelitian ini tiga tahap proses derivatisasi mampu menghasilkan pemisahan
peak yang baik meskipun asam glukuronat tidak terdeteksi pada sampel (Saraiva et al., 2011).
b. Berat molekul komponen: massa molar
ramnosa yaitu 164,1565 g/mol (paling ringan dibanding komponen lain) sedangkan
massa molar asam galakturonat yaitu 194,139 g/mol (paling berat dibanding
komponen lain), sehingga ramnosa memiliki RT paling pendek dan asam
galakturonat memiliki RT paling panjang (PubChem, 2017).
c. Injeksi sampel: Sampel diinjeksikan
secara langsung sebanyak 1 վL tanpa splitting. 100% sampel yang telah
diinjeksikan akan diuapkan pada suhu 250oC dalam injektor dan masuk
ke dalam kolom (Yuliati dkk, 2012).
d. Jenis kolom: jenis kolom yang digunakan
yaitu kolom kapiler DB-17 yang merupakan kolom dengan fase stasioner (fase
diam) fenil 50%-metilpolisiloksan 50% yang bersifat semi polar dan dapat
dioperasikan pada range suhu 40-280/300oC (Agilent, 2017).
e. Gas pembawa (carrier gas): Gas pembawa
harus sangat murni atau Ultra High Purity (UHP) dan dialirkan dengan kecepatan
tertentu. Semakin cepat aliran maka kecepatan migrasi solut semakin cepat. Gas
pembawa yang digunakan adalah jenis N2 dengan kecepatan alir 1,5
mL/menit dan hidrogen sebagai gas pendorong dengan kecepatan alir 60 mL/menit
(Li et al., 2015).
f. Ketebalan fase stasioner: Semakin tebal
fase stasioner maka resolusi dua komponen yang terelusi secara berurutan juga
meningkat. Fase stasioner yang tebal akan meretensi komponen lebih lama dan
memerlukan suhu yang lebih tinggi untuk mengelusi komponen pada nilai k’ yang
sama. Pada penelitian ini ketebalan fase stasioner yaitu 0,25 mm (ketebalan
standar) dan sesuai untuk pemisahan solut yang terleusi hingga suhu 300oC
(Saraiva et al., 2011).
g. Panjang kolom: semakin panjang kolom
maka pemisahan solut pada sampel semakin baik. Hal ini karena resolusi kolom
akan meningkat seiring dengan semakin panjang kolom (Li et al., 2015).
h. Suhu kolom dan Gradien suhu: Semakin
tinggi suhu kolom maka interaksi solut dengan fase stasioner semakin lemah.
Karena itu adanya gradien suhu bertujuan agar peak yang terbentuk berdekatan
(range waktu munculnya peak tidak terlalu jauh) akibat interaksi solut dengan
fase stasioner yang melemah seiring meningkatnya suhu (Yuliati dkk, 2012).
i. Detekor: detektor yang digunakan yaitu
FID yang merupakan detektor general untuk mengukur solut sampel yang memiliki
gugus alkil (C-H). Gas pembakar yang digunakan yaitu campuran udara dan H2.
Selain itu, FID merupakan detektor yang sesuai dengan gas N2 yang
merupakan gas pembawa. Batas deteksi minimum (BDM) yang disepakati adalah
sebesar 10-12. Asam glukuronat terdapat dalam jumlah kurang dari 10-12
di dalam sampel sehingga tidak terdeteksi detektor (Li et al., 2015).
4. Referensi
Jurnal Utama
Wang,
X., Zhang, L., Wu, J., Xu, W., Wang, X., Lü, X. (2017). Improvement of Simultaneous Determination of Neutral Monosaccharides
and Uronic Acids by Gas Chromatography. Food Chemistry 220 (2017) 198–207.
Literatur Pendukung
Agilent.
(2017). DB-17 Column. Diakses
melalui http://www.agilent.com
pada 25 November 2017.
Huang,
Y., Li, N., Wan, J.-B., Zhang, D., & Yan, C. (2015). Structural Characterization and Antioxidant Activity of A Novel
Heteropolysaccharide from The Submerged Fermentation Mycelia of Ganoderma capense. Carbohydrate
Polymers, 134, 752–760.
Li,
W.-Y., Li, P., Li, X.-Q., Huang, H., Yan, H., Zhang, Y., et al. (2015). Simultaneous Quantification of Uronic Acid,
Amino Sugar, and Neutral Sugar In The Acidic Polysaccharides Extracted from The
Roots of Angelica sinensis (Oliv.) Diels
by HPLC. Food Analytical Methods, 8(8), 2087–2093.
Mao,
G.-H., Ren, Y., Feng, W.-W., Li, Q., Wu, H.-Y., Jin, D. (2015). Antitumor and Immunomodulatory Activity of
A Water-Soluble Polysaccharide from Grifola
frondosa. Carbohydrate Polymers, 134, 406–412.
PubChem.
(2017). D-Galacturonic Acid. Diakses
melalui https://pubchem.ncbi.nlm.nih.gov
pada 25 November 2017.
Saraiva,
D., Semedo, R., Castilho, Mda C, Silva, J.M., Ramos, F. (2011). Selection of The Derivatization Reagent-The
Case of Human Blood Cholesterol, Its Precursors and Phytosterols GC-MS analyses.
J Chromatogr B. 879:3806-11.
Yang,
L., and Zhang, L.-M. (2009). Chemical
Structural and Chain Conformational Characterization of Some Bioactive
Polysaccharides Isolated from Natural Sources. Carbohydrate Polymers,
76(3), 349–361.
Yuliati,
W., M. Ilyah, K. Indirawati. (2012). Analisa
Kinerja Gas Chromatography Tipe Shimadzu GC-FID 2010 Pada Pengaruh Perubahan
Temperature Column Terhadap Nilai Retention Time dan Area of Detection Peak dari
Bhypenile in N-Hexane di PT. Ditek Jaya (SHIMADZU Analytical and Scientific
Corp.). Jurnal Teknik Fisika Vol. 1, No. 1, (2012) 1-5.
Zhang,
Z., Khan, N. M., Nunez, K. M., Chess, E. K., and Szabo, C. M. (2012). Complete Monosaccharide Analysis by
High-Performance Anion-Exchange Chromatography with Pulsed Amperometric
Detection. Analytical Chemistry, 84 (9), 4104–4110.






No comments:
Post a Comment